ЭНДОКРИНОЛОГИЯ - EURODOCTOR.ru -2005
Семенники (яички) это мужские половые железы. В семенниках образуются мужские половые клетки – сперматозоиды, и мужские половые гормоны (андрогены) регулирующие у мужчин функции пола.
Яички состоят из системы сперматогенных канальцев. Здесь образуются и отсюда транспортируются сперматозоиды.
Мужские стероидные половые гормоны вырабатываются в яичках специальными клетками, которые называются клетки Лейдига. Синтезируются мужские половые гормоны из холестерина путем различных химических превращений при помощи ферментов.
Регулирует функции мужских половых органов гипоталамус, который расположен в головном мозге. В ядрах гипоталамуса вырабатывается гонадолиберин. У мужчин выработка этого гормона происходит постоянно, в отличие от циклической его секреции у женщин. Гонадолиберин оказывает стимулирующее действие на гипофиз (расположенный в головном мозге), в котором происходит продукция сначала лютропина (лютеинизирующий гормон), затем фоллитропина (фолликулостимулирующий гормон). Под действием лютропина в яичках происходит синтез и выделение тестостерона, а фоллитропин стимулирует образование сперматозоидов. Выброс гонадолиберина гипоталамусом регулируется по принципу обратной связи. Снижают выделение этого гормона в кровь: высокая концентрация самого гонадолиберина, высокая концентрация фоллитропина и лютропина и высокая концентрация тестостерона и эстрогенов, которые и являются конечным звеном этой цепи.
Таким образом половые гормоны сами регулируют скорость своей продукции. Синтезируются в яичках тестостерон и некоторое количество эстрогенов (женские половые гормоны).
Тестостерон , образовавшийся в яичках транспортируется по организму при помощи белков-переносчиков. В тканях организма из тестостерона образуются два вида более активных гормонов – дигидротестостерон и небольшое количество эстрогенов.
Дигидротестостерон и является основным мужским половым гормоном, который отвечает за многие вторичные мужские половые признаки.
Концентрация эстрогенов в мужском организме увеличивается с возрастом и при увеличении массы тела, так как эстрогены активнее производятся в жировой ткани. Основные функции мужских половых гормонов (андрогенов) – формирование мужских половых признаков и поддержание функции размножения. К моменту рождения концентрация тестостерона у мальчиков только незначительно выше, чем у девочек.
После рождения уровень тестостерона у мальчиков быстро повышается, затем к первому году жизни снижается, и до подросткового периода остается низкой. В подростковом периоде количество тестостерона повышается и к 17 годам достигает уровня взрослых. Начиная с 17 лет уровень тестостерона в крови мужчин практически постоянный до 60 лет. С 60 лет начинается его постепенное снижение.
Под действием мужских половых гормонов происходит:
- формирование и рост придатков яичек, семенных пузырьков, предстательной железы, полового члена,
- оволосение по мужскому типу (усы, борода, волосы на туловище и конечностях, оволосение в виде ромба на лобке)
- увеличивается гортань
- утолщаются голосовые связки (тембр голоса при этом снижается)
- ускоряется рост мышц и рост всего тела.
К завершению полового созревания таким образом уровень андрогенов достигает уровня взрослого мужчины, а продукция сперматозоидов в состоянии обеспечить оплодотворение.
Процесс образования сперматозоидов в яичках чрезвычайно чувствителен ко всякого рода неблагоприятным воздействиям. Производство сперматозоидов (сперматогенез ) снижается при действии:
- повышенной температуры
- психологических стрессов
- при приеме некоторых лекарственных препаратов.
Недостаток андрогенов в раннем внутриутробном периоде приводит к различным аномалиям развития половых органов:
- микрофаллос.
Если недостаток андрогенов возникает до подросткового возраста, формируется «евнухоидизм».
- При этом не происходит полового созревания у ребенка мужского пола.
- У пациента слабое развитие мышц, на теле нет или мало волос, нарушено формирование костей.
- В результате нарушения формирования костного скелета размах рук превышает рост на несколько санитиметров.
Если недостаток андрогенов возникает после подросткового периода, когда процесс полового созревания завершился, то большинство развившихся вторичных половых признаков сохраняется. Рост бороды, например, практически не изменяется. Остальные признаки могут медленно регрессировать.
- Развивается нарастающая импотенция , исчезают спонтанные и вызванные адекватным раздражителем эрекции.
- Уменьшаются размеры яичек, снижается мышечная сила.
- Все это сопровождается нарушениями в психо-эмоциональной сфере вплоть до развития депрессии.
Состояние, сопровождающееся недостаточностью функции мужских половых желез (яички) с нарушением образования половых гормонов и сперматозоидов называется гипогонадизмом .
Половые железы человеческого организма исполняют ряд важных функций: определяют физиологические особенности пола и отвечают за размножение. Они характеризируются смешанным типом секреции, так как вырабатывают и половые клетки, и специфические гормоны. Женские и мужские гонады имеют некоторые особенности. Тем не менее, регуляция деятельности желез осуществляется гонадотропными
Мужские половые железы . Половые железы мужчины представлены яичками, в которых вырабатывают сперматозоиды (половые клетки), а также андрогены (специфические мужские гормоны).
Процессы сперматогенеза происходят в так называемых клетках Лейдига. Образование сперматозоидов идет практически непрерывно — начиная с и заканчивая возрастом 50 - 60 лет (это индивидуальные данные), когда семенники атрофируются, и их физиологическая активность медленно затухает. Созревают половые клетки в
Мужской сперматозоид состоит из головки, шейки, хвоста и жгутика, с помощью которого он может передвигаться. На головке клетки имеется так называемая акросома, в которой содержатся ферменты, разрушающие оболочку яйцеклетки. В женском влагалище сперматозоид может быть активен до 6 суток.
Что же касается половых гормонов, то самым важным является тестостерон, продукция которого регулируется гипофиза. Этот гормон имеет огромное значение в развитии мужского организма, так как отвечает за:
- увеличение и активное развитие половых органов во время полового созревания;
- развитие оволосения по мужскому типу;
- голоса;
- активный рост и развитие мышц;
- формирование костей;
- появление влечения к людям противоположного пола;
Как можно заметить, половые железы у мужчин исполняют довольно важные функции. Например, при нарушении процессов сперматогенеза человек не способен произвести потомство. А при недостатке половых гормонов развивается так называемый евнухоидизм — у мужчины наблюдается отложение жира на груди, бедрах и ягодицах, части тела растут непропорционально, половые органы остаются недоразвитыми, отсутствует половое влечение, развиваются психологические отклонения.
Женские половые железы . Гонады женщин представлены яичниками, в которых созревают яйцеклетки и синтезируются женские и прогестерон. Каждый женский яичник состоит из двух шаров: стромы и коркового вещества.
Фолликулы с яичниками на разных стадиях созревания расположены в корковом веществе. И если у мужчин процесс образования сперматозоидов идет в течение всей жизни, то у женщин все половые клетки закладываются еще во время эмбрионального развития. В месяц созревает только одна яйцеклетка, которая разрывает фолликул и двигается по фаллопиевой трубе. На месте фолликула образуется которое затем превращается в белое, в последующем на месте вышедшей яйцеклетки остается небольшой рубец.
Половые железы у женщин продуцируют и специфические гормоны: прогестерон и эстрогены. Эстрогены выполняют ряд функций:
- отвечают за увеличение внешних и внутренних половых органов во время полового созревания;
- формируют женский тип оволосения;
- ускоряют развитие молочных желез;
- тормозят рост костей в длину;
- стимулируют процессы синтеза жиров, которые за тем откладываются на груди, животе, бедрах и ягодицах — это особенности женского телосложения;
Прогестерон выделяется желтым телом. Его основная функция — это подготовка эндометрия матки к внедрению оплодотворенной яйцеклетки. Этот гормон также влияет и на молочные железы, вызывая их набухание.
Если половые железы женщины работают неправильно, то это чревато бесплодием, задержкой полового развития, психологическими травмами.
В функциональном отношении тесно связанные между собой половые органы мужчины подразделяются на: 1) половые железы - яички (семенники); 2) дополнительные половые образования (придаточные половые железы); 3) половые пути (семявыводящие пути); 4) органы совокупления.
Физиология яичек . Яички одновременно выполняют двойную функцию: герминативную и внутрисекреторную. Герминативная функция за счет сперматогенеза обеспечивает образование мужских половых клеток (спермиев), способствуя тем самым продолжению рода.
Внутрисекреторная функция заключается в выделении мужских половых гормонов (андрогенов), среди которых основным является тестостерон. Помимо андрогенов, в яичке образуются эстрогены, главным образом эстрадиол.
Тестостерон является наиболее активным андрогенным гормоном. Местом синтеза андрогенов у мужчин являются гландулоциты яичка (клетки Лейдига), расположенные в интерстициальной ткани яичек поодиночке или группами. Гландулоциты имеют значительные размеры, правильную форму и содержат в цитоплазме липоидные и пигментные включения. Тестостерон способствует возникновению вторичных половых признаков и либидо, созреванию мужских половых клеток - спермиев, - обладает выраженной анаболической активностью, стимулирует эритропоэз, существенно влияет на синтез белка, индуцирует ферменты. В больших дозах андрогены тормозят пролиферацию хрящевой ткани и стимулируют ее оссификацию; дефицит гормонов приводит к торможению процессов окостенения хряща. Под влиянием тестостерона, вырабатываемого яичками плода, происходят маскулинизация наружных и внутренних половых органов и развитие их по мужскому типу.
Средняя суточная продукция тестостерона в организме мужчин 25-40 лет колеблется, по данным О. Н. Савченко (1979), в пределах 4-7 мг.
Максимальная продукция андрогенов половыми железами наблюдается у мужчин в возрасте 25-30 лет, после этого начинается медленное снижение их гормональной активности. При старении уровень тестостерона в крови снижается, уровень эстрогенов - повышается.
На основании собственных исследований и изучения обширной литературы У. Мейнуоринг (1979) пришел к следующим выводам. Основной андроген (тестостерон) циркулирует с кровью в виде устойчивого комплекса с белками плазмы и подвергается интенсивному метаболизму только в клетках-мишенях для андрогенов. Основным его метаболитом является 5α-дегидротестостерон.
5α-дегидротестостерон представляет собой активный метаболит тестостерона, который с белками плазмы образует андрогенрецепторный комплекс, способный связываться с ядерными акцепторами и стимулировать многие биохимические процессы. Разрушение и вытеснение из ядра андрогенрецепторного комплекса приводит к замедлению основных биохимических процессов, обусловливающих андрогенный ответ.
Метаболизм тестостерона происходит под действием специального фермента 5α-редуктазы. В мужских добавочных половых железах содержится значительное количество 5α-редуктазы, при участии которой в них возможно образование 5α-дегидротестостерона. Было также установлено, что 5α-дегидротестостерон прочно связывается с ядрами клеток добавочных половых желез. В придаточных половых железах, мышцах и других тканях расположены клетки-мишени, которые являются акцепторами для тестостерона и его метаболитов и способны давать специфические андрогенные ответы.
Андрогены яичек плода вызывают регресс мюллеровых протоков и развитие из вольфовых протоков придатков яичек, семявыносящих протоков, семенных пузырьков, предстательной железы с маскулинизацией наружных половых органов.
Добавочные половые железы постоянно испытывают на себе влияние андрогенов, которые способствуют их правильному формированию и нормальному функционированию.
Тестостерон стимулирует образование фруктозы в семенных пузырьках, лимонной кислоты и фосфатазы в предстательной железе, корнитина в придатках яичка и пр.
Уменьшение содержания в семенной жидкости фруктозы, лимонной кислоты, кислой фосфатазы, корнитина может указывать на снижение внутрисекреторной функции яичек.
Обнаружено, что приблизительно через 7-10 дней после двусторонней орхиэктомии мужские добавочные половые железы у грызунов атрофируются до минимума. Последующее введение тестостерона приводит к значительному увеличению их массы и усилению внутриклеточной секреции.
Таким образом, биологические ответы на андрогены направлены на поддержание структуры и функции андрогенных клеток-мишеней, типичным примером которых являются клетки мужских добавочных половых желез.
Изучение механизма действия гормонов осложняется взаимопревращением андрогенов в эстрогены и андростендиола (основного андрогеноподобного стероида, секретируемого надпочечниками) в тестостерон.
В настоящее время не вызывает сомнений, что некоторые биохимические явления специфически регулируются самим тестостероном, другими активными метаболитами и даже эстрогенами.
80% эстрогенов у мужчин образуется в яичках и лишь 20% - в надпочечниках. Биологическое значение эстрогенов в мужском организме заключается в стимулирующем влиянии на интерстициальные клетки половых желез, гладкую мускулатуру, соединительную ткань и специфический эпителий.
Большое значение в организме человека придается антиандрогенам. У. Мейнуоринг (1979) отмечает антиандрогенное действие эстрогенов, основанное на подавлении секреции гонадотропинов, ингибировании системы 5α-редуктазы и стимуляции синтеза половых стероидных гормонов. В какой-то степени эстрадиол может конкурировать с 5α-дегидротестостероном за связывающие места, но только в том случае, если присутствует в избытке.
Андрогенные стероиды вырабатываются как яичками, так и надпочечниками. "Корой надпочечников вырабатываются производные андростана, обладающие андрогенной активностью: 17-кетостероиды (дегидроэпиандростерон, этиохоланолон, андростендион, андростерон) - и мужской половой гормон тестостерон, а также производные эстрана - эстрогены (эстрадиол и эстрон). Важным промежуточным продуктом синтеза гормонов коры надпочечников является прогестерон. Значительная часть андрогенов, претерпевая изменения, выделяется почками в виде нейтральных 17-кетостероидов (17-КС).
Из общего количества 17-КС, выделяемых с мочой, 1 / 3 образуется за счет метаболизма соединений, продуцируемых клетками Лейдига яичка, а 2 / 3 - клетками коры надпочечников. Понятно, что колебания уровня экскреции 17-КС зависят от состояния ЦНС и системы гипоталамус - гипофиз - надпочечники. На самом деле определение 17-КС в моче дает лишь общие сведения о метаболизме стероидных соединений, вырабатываемых и яичками, и корой надпочечников. Поэтому определение выделения 17-КС с мочой не может служить методом оценки эндокринной функции гландулоцитов яичка.
Таким образом, становится понятно, что только прямое определение тестостерона и эстрадиола в крови и моче, являющихся в основном продуктами яичек (в мужском организме), может служить показателем гормональной функции яичек.
Одной из важнейших функций андрогенов и в особенности тестостерона является поддержание процесса сперматогенеза. Состояние сперматогенеза зависит от концентрации андрогенов в тестикулярной ткани, и потому снижение образования тестостерона может быть одной из основных причин неплодовитости мужчин.
Для полного течения процесса сперматогенеза важна также роль андроген-связывающего белка, который образуется в яичках и способствует переносу андрогенов в цитоплазму клеток сперматогенного эпителия. Цитоплазматический рецептор, соединяясь с андрогенами, облегчает их проникновение непосредственно в ядра.
Сперматогенез. Процесс сперматогенеза осуществляется в извитых семенных канальцах паренхимы яичка, которые составляют основную объемную массу его. Внутренняя поверхность мембран извитых канальцев выстлана двумя видами клеток, сустентоцитами и первичными половыми клетками - сперматогониями. Именно здесь недифференцированные семенные клетки сперматогонии размножаются и превращаются в зрелые спермии.
В течение эмбрионального развития и в детском возрасте первичные сперматогонии делятся митотически, давая начало дополнительным сперматогониям. С 10-летнего возраста в семенных канальцах мальчиков начинаются усиленное митотическое деление сперматогоний и формирование сустентоцитов. Начальные этапы сперматогенеза появляются в 12-летнем возрасте - происходит образование сперматид из сперматоцитов второго порядка. Полное формирование сперматогенеза происходит к 16 годам.
Изнутри мембрану семенного канальца выстилают сустентоциты, которые обеспечивают сперматогенные клетки продуктами своей секреторной активности, выполняют фагоцитарную функцию в отношении остатков после сперматогенеза, синтезируют эстрогеноподобное вещество (ингибин), выделяют андрогенсвязывающий протеин, способствующий переносу тестостерона и дигидротестостерона в половые клетки, где они закрепляются в ядре, обусловливая различные метаболические процессы, необходимые для созревания спермиев. Как бы втиснутые между сустентоцитами, ближе к основанию мембраны располагаются сперматогонии. В просвет канальца направлены многочисленные цитоплазматические отростки сустентоцитов, между отростками располагаются клетки сперматогенного эпителия. По мере созревания клетки сперматогенного эпителия продвигаются к просвету канальца. В результате митотического деления приумножается число сперматогоний. Последние, увеличиваясь в размерах, превращаются в сперматоциты первого порядка, каждый из которых содержит диплоидный набор хромосом 46XY. Сперматоциты первого порядка после усиленного роста и созревания вступают в стадию мейоза (редукционного деления). При этом из сперматоцитов первого порядка образуются 2 сперматоцита второго порядка с гаплоидным набором хромосом (22 аутосомы и 1 половая - X или Y). Из каждого сперматоцита второго порядка образуются путем быстрого митотического деления 2 сперматиды. В конечном итоге из одного сперматоцита первого порядка образуются четыре сперматиды, содержащие уменьшенный наполовину гаплоидный набор хромосом. Сперматиды захватываются цитоплазматическими выростами сустентоцитов, в цитоплазме которых происходит развитие и формирование спермиев. Сперматида удлиняется, ядро ее смещается эксцентрично. Из части цитоплазмы формируется шейка и вырастает жгутик спермия. После распада протоплазменных выростов сустентоцитов спермии освобождаются и выходят в просвет канальцев, накапливаются в придатке, где происходит их дозревание.
Развитие и дифференциация спермиев проходят 3 этапа: 1) пролиферация сперматогоний - сперматоцитогенез, 2) деление и созревание сперматоцитов - сперматогенез и 3) конечная фаза, дифференциации сперматид в спермии - спермиогенез. Профаза первого (мейотического) деления сперматоцита 1-го порядка занимает значительную долю (около 3 / 8) времени сперматогенеза. Второе (митотическое) деление сперматоцитов 2-го порядка, приводящее к образованию сперматид, происходит довольно быстро. Морфологические изменения в сперматиде, включающие в себя перестройку ядра и цитоплазматических элементов и завершающиеся образованием спермиев, суммарно описываются как спермиогенез и также длятся около 3/8 времени сперматогенеза (рис. 4). Время, необходимое для превращения первичной клетки в спермий, занимает у человека около 74-75 дней. Жидкость, заполняющая просвет семенных канальцев, представляет собой продукт секреции клеток семенных канальцев и содержит гормон (ингибин), который угнетает продукцию фолликулостимулирующего гормона (ФСГ) гипофизом. При поражении семенных канальцев и угнетении сперматогенеза уменьшается продукция ингибина, это приводит к повышенному выделению гонадотропинов гипофизом.
В зародышевом эпителии яичек образуется фермент гиалуронидаза, которая локализуется в головке спермиев. Небольшое количество гиалуронидазы попадает в плазму эякулята из спермиев. Гиалуронидаза растворяет слизь шейки матки и обладает свойством разъединять клетки лучистого венца (corona radiata) яйцеклетки без их деструкции и таким образом создавать возможность для внедрения в нее спермия. Значительная концентрация гиалуронидазы создается достаточным количеством спермиев. При аспермии гиалуронидаза в эякуляте отсутствует.
Другим продуктом секреции яичек являются простагландины, открытые шведским ученым Euler в 1936 г. Предполагалось, что они образуются в предстательной железе. Затем было установлено, что основным местом их образования являются яички. Было доказано влияние простагландинов на сократительную способность гладкой мускулатуры и стимулирующее влияние на выработку ФСГ и ЛГ. Из выделенных в настоящее время нескольких десятков простагландинов практическое значение имеют два вида: Е 2 - очень неустойчивый и Е 2α - стойкий. В больших объемах эякулята содержится большее количество простагландинов. Их способность расслаблять и сокращать гладкую мускулатуру женских половых путей повышает скорость прохождения яйцеклетки через маточные трубы навстречу спермиям в процессе зачатия. Высокое содержание простагландинов стимулирует сократительную способность гладкой мускулатуры матки, прерывая беременность.
Базальная мембрана канальцев (особенно мышечноподобные клетки внутреннего слоя и сустентоциты) создают гематотестикулярный барьер, защищающий генеративный эпителий, ответственный за наследственность и продление рода, от инфекционных и токсических поражений.
Исследование эякулята позволяет судить о степени и характере нарушений внутрисекреторной и экскреторной функций яичек, так как тестостерон и гонадотропины влияют на морфологические и физико-химические свойства эякулята.
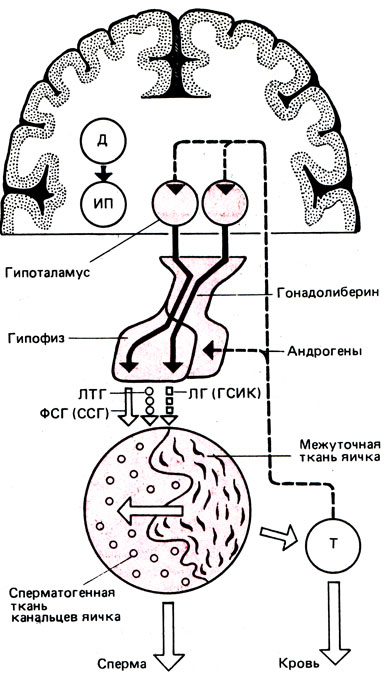
Регуляция функции яичек. Деятельность яичек находится непосредственно под влиянием ЦНС, гипоталамуса и гипофиза. Кора головного мозга выполняет наиболее ответственную функцию - приспособление деятельности эндокринной системы к постоянно изменяющимся факторам внешней и внутренней среды. Действие коры головного мозга на половые железы реализуется через гипоталамус - гипофиз или через изменение функционального состояния вегетативной нервной системы, приводящее к расстройствам кровообращения. Надо полагать, что, наряду с нарушением васкуляризации, нарушается обмен веществ в иннервируемом органе (яичках), что и приводит к нарушению сперматогенеза.
Роль нервной системы и гипоталамических центров при регулировании функций мужских половых желез заключается в их влиянии, осуществляемом не только нейрогенным путем, но и через секрецию гипофиза, гормоны которого стимулируют функцию яичек. Гормоны, выделенные нервными клетками и определенными ядрами гипоталамуса, доставляются к гипофизу и стимулируют выделение гонадотропных гормонов.
Гипоталамус и гипофиз следует рассматривать как комплекс двух тесно связанных желез внутренней секреции (рис. 5). Рилизинг-гормон, вырабатываемый гипоталамусом, оказывает прямое влияние на стимуляцию или торможение секреции гормонов гипофиза. Выработка гонадотропин-рилизинг-гормона происходит преимущественно в области аркуатных ядер и стимулируется дофамином. Серотонин, выделяемый эпифизом, тормозит продукцию рилизинг-гормона. У мужчин функционирует постоянный тонический центр секреции рилизинг-гормона, у женщин - циклический. Такая половая дифференцировка гипоталамуса происходит во внутриутробном периоде под влиянием вырабатываемого эмбриональными яичками тестостерона.
В настоящее время установлено, что синтез и выделение гонадотропных гормонов регулируются единым гонадотропин-рилизинг-гормоном. М. Ammos и A. Sehally (1971) осуществили его синтез. Передняя доля гипофиза секретирует 3 гонадотропных гормона, которые оказывают влияние на функцию семенников.
ФСГ, именуемый в мужском организме сперматогенезстимулирующим гормоном (ССГ), активно влияет на сперматогенез, стимулирует эпителий канальцев яичка. ЛГ у мужчин инициирует развитие, созревание интерстициальных клеток и влияет на биосинтез андрогенов, поэтому носит название гормона, стимулирующего интерстициальные клетки (ГСИК).
Роль третьего гормона - пролактина, или лютеотропного гормона (ЛТГ), - в мужском организме долгое время оставалась неизвестной. Исследования последних лет показали, что пролактин является гормоном широкого спектра действия, в том числе и регулятором половой функции у мужчин. Пролактин потенцирует действие ЛГ и ФСГ, направленное на восстановление и поддержание сперматогенеза, увеличивает массу семенников и семенных канальцев, под влиянием пролактина усиливаются обменные процессы в яичке. Совместное назначение ЛГ и пролактина значительно больше повышает содержание тестостерона в плазме крови, чем при назначении только ЛГ. Пролактин подавляет образование дегидротестостерона.
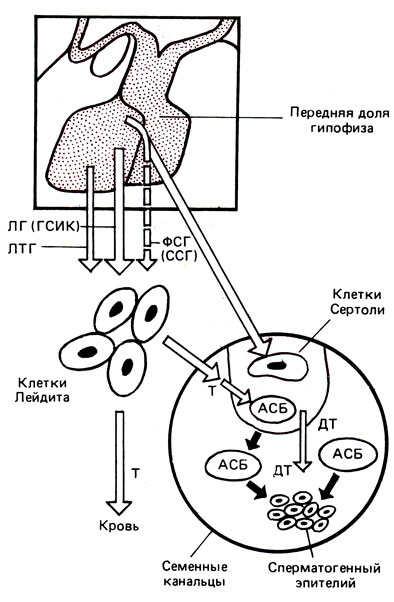
Подавление образования дегидротестостерона из тестостерона в предстательной железе под влиянием пролактина осуществляется за счет торможения активности 5α-редуктазы. Изменяя таким образом обмен андрогенов, пролактин стимулирует секрецию предстательной железы по сравнению с ее ростом. У человека отчетливо прослеживается зависимость между содержанием пролактина в эякуляте и числом подвижных спермиев. В зависимости от степени снижения концентрации пролактина отмечаются низкая подвижность спермиев, олиго- или азооспермия. Процесс сперматогенеза у человека и животных прекращается после выключения гипофиза. В таких случаях сперматогенез блокируется уже на этапе сперматоцитов 1-го порядка еще до редукционного деления. Считают, что ФСГ стимулирует рост семенных канальцев, функцию клеток Сертоли, инициирует митотическую фазу сперматогенеза (от сперматогоний до сперматоцитов). Под влиянием ЛГ функционируют клетки Лейдига, вырабатывая тестостерон, который обеспечивает заключительную фазу сперматогенеза (спермиогенез) - превращение сперматоцитов в сперматиды и созревание их в спермии (рис. 6).
С другой стороны, андрогены действуют на диэнцефальную область, оказывают стимулирующее действие также на высшие корковые центры. При этом усиливаются положительные условные рефлексы и повышается тонус коры головного мозга.
Андрогены и эстрогены при длительном введении в больших дозах приводят к торможению нейросекреции гипоталамуса, к исчезновению гонадотропинов и к расстройствам сперматогенеза. Разрушение рецепторной (для половых стероидов) зоны гипоталамуса приводит к состоянию, имитирующему посткастрационное, что объясняется выключением афферентного звена в механизме обратной связи. Это свидетельствует о том, что местом приложения половых стероидов является передний гипоталамус, и объясняет также механизм развития бесплодия при некоторых диэнцефальных поражениях. Секреция ФСГ регулируется частично некоторыми неандрогенными факторами, имеющими неспецифическую связь со сперматогенезом, и частично тестостероном и его метаболитами. Поэтому при тяжелом, нарушении сперматогенеза вследствие крипторхизма наблюдается повышение уровня ФСГ в сыворотке крови. Установлена обоюдная количественная корреляция между уровнями ФСГ и тестостерона, что указывает на отрицательную регуляцию по типу обратной связи, существующей между ФСГ и тестостероном. Нарушение обратной чувствительности гипоталамоипофизарной системы к уровню периферического тестостерона (имеющее место при синдроме Клайнфелтера), чрезмерное повышение секреции гонадотропина приводят к вторичным изменениям гландулоцитов яичка и снижению уровня тестостерона. Таким образом, существование автоматической регуляции гипоталамической деятельности гипофиза и яичек является важным биологическим процессом, управляющим сперматогенной и инкреторной функцией половых желез.
Придаток яичка - представляет собой андрогензависимый, секреторно-активный орган, который служит для проведения накопления и дозревания спермиев. В придатке яичка под действием андрогенов создается благоприятная среда для завершения их развития и жизнедеятельности. По мере продвижения от головки до хвоста, продолжающегося в норме 14 дней, происходит окончательное морфологическое, биохимическое и физиологическое созревание спермиев, обретающих способность двигаться и оплодотворять яйцеклетку. В придатке спермин освобождаются от цитоплазматической капли (остатки цитоплазмы сустентоцитов), обволакиваются защитной белковой оболочкой, приобретают отрицательный заряд и насыщаются секретом, содержащим гликоген, жиры, холестерин, фосфаты, корнитин и др., происходит ряд ультраструктурных и цитохимических преобразований акросомы. По мере продвижения и созревания спермии накапливаются в хвосте, который является для них хранилищем. Концентрация спермиев здесь может быть в 10 раз больше, чем в нормальном эякуляте. Слабое напряжение кислорода и отсутствие фруктозы препятствуют активному метаболизму в спермиях и способствуют длительному сохранению их жизнедеятельности. При половом воздержании в хвосте придатка могут обнаруживаться и старые, переродившиеся формы спермиев. Эпителий придатка способен дезинтегрировать и абсорбировать нежизнеспособные формы спермиев. В этом процессе значительную роль играют спермиофаги. Способность к поглощению и усвоению спермией создает условия для поддержания сперматогенеза у больных с обструктивной аспермией, при частичном сохранении функционирующей части придатка. При полном поражении придатка яичка сперматогенез нарушается, так как наступают переполнение и гибель канальцев яичка. Продвижение спермиев из яичек в придаток и в самом придатке осуществляется за счет движения ресничек мерцательного эпителия выносящих канальцев и давлением непрерывно поступающего секрета яичка.
Семявыносящий проток является органом, служащим для проведения спермиев от хвоста придатка до ампулы семявыносящего протока, где происходит их накопление. При половом возбуждении спермии могут накапливаться также и на длинном отрезке между ампулой и хвостовой частью придатка яичка. При эякуляции опорожняются прежде всего ампула и периферический отрезок семявыносящего протока. Содержимое семявыносящего протока проталкивается во время эякуляции по направлению к уретре за счет укорочения всего придатка в результате сокращения его мощной мускулатуры. При последующих извержениях количество спермиев значительно уменьшается и поступают они из хвоста придатка яичка, который полностью никогда не опорожняется.
Семенные пузырьки являются железистыми андрогензависимыми секреторными органами. Секрет семенных пузырьков состоит из вязкой, беловато-серой желатиноподобной субстанции, которая после эякуляции разжижается в течение нескольких минут и составляет около 50-60% семенной жидкости. Наиболее важной функцией семенных пузырьков является секреция фруктозы, уровень которой является показателем андрогенной насыщенности организма. Фруктоза служит источником энергии, метаболизма и поддержания подвижности спермиев. Нормальное содержание фруктозы в сперме здорового мужчины 13-15 ммоль/л. При хранении эякулята количество фруктозы уменьшается из-за потребления ее спермиями. Расходование фруктозы спермиями (фруктолиз) в нормальном эякуляте не ниже 3-5 ммоль/л за 2 ч. Семенные пузырьки секретируют и другие составные части спермы: азотистые вещества, белки, инозит, аскорбиновую кислоту, простагландины и др. Секрет семенных пузырьков с рН 7,3, примешиваясь к секрету яичек, играет роль защитного коллоида, придавая спермиям большую сопротивляемость. При нереализованном половом возбуждении спермии попадают в семенные пузырьки, где они могут поглощаться клетками-спермиофагами. Семенные пузырьки также способны к резорбции жидких компонентов.
Предстательная железа - андрогензависимый орган, поставляющий около 25-35% плазмы спермы. При уменьшении уровня андрогенов в крови ее секреторная активность значительно снижается. Слабощелочной секрет предстательной железы в норме содержит значительное количество преломляющих свет зернышек (липоидных телец), которые придают ему опалесцирующий беловатый оттенок. Значительное содержание в секрете предстательной железы спермина придает эякуляту характерный запах. При медленном охлаждении в эякуляте появляются кристаллы фосфата спермина. Фибринолизин и фиброгеназа, являясь мощными протеолитическими ферментами, принимают участие в разжижении эякулята.
В предстательной железе также образуется лимонная кислота, концентрация которой служит показателем функционального состояния ее и своеобразным "андрологическим эквивалентом" эндокринной функции яичек.
В норме концентрация лимонной кислоты в семенной жидкости колеблется от 2,5 до 3,5 ммоль/л. Секрет предстательной железы содержит кислую и щелочную фосфатазы. Отношение содержания кислой фосфатазы к щелочной (фосфатазный индекс) является довольно стабильной величиной [Юнда И. Ф., 1982]. Под действием фосфатазы происходит расщепление холин-фосфорной кислоты семенной плазмы на холин и фосфорную кислоту. Спермин, соединяясь с фосфорной кислотой, образует кристаллы фосфорного спермина. Холин оказывает сенсибилизирующее действие на клетки. Спермин и спермидин, являясь основаниями, поддерживают на постоянном уровне концентрацию водородных ионов. В предстательной железе вырабатываются простагландины, влияющие на сократительную деятельность гладкой мускулатуры. Высказывается мнение об эндокринной функции предстательной железы. Однако убедительные данные в пользу этого до сих пор отсутствуют. В клетках-мишенях предстательной железы происходит метаболизм тестостерона. Под действием 5α-редуктазы тестостерон превращается в еще более активный метаболит 5α-дегидротестостерон, способный с белками плазмы образовывать андрогенрецепторный комплекс, который может проникать в ядерные структуры и стимулировать многие биохимические процессы.
Приведенные данные показывают, что предстательная железа увеличивает объем эякулята, участвует в разжижении, оказывает буферное и ферментативное действие на эякулят в целом и активизирует движение спермиев. Функционально предстательная железа тесно связана с семявыводящими путями. Патологические изменения в ней могут приводить к нарушениям репродуктивной и копулятивной функций. Размеры предстательной железы значительно меняются с возрастом. Железистая ткань ее развивается в период полового созревания и дегенерирует у стариков.
Луковично-уретральные железы являются гомологом бартолиновых желез. Секрет этих желез, выделяющийся в мочеиспускательный канал при половом возбуждении за счет сокращения мышц промежности, представляет собой бесцветную прозрачную, лишенную запаха слизь со щелочной реакцией. При прохождении по уретре секрет нейтрализует кислую реакцию остающейся в ней мочи и, выделяясь из наружного отверстия мочеиспускательного канала, облегчает введение полового члена во влагалище. С возрастом отмечается гипотрофия луковично-уретральных желез.
Уретральные железы . На всем протяжении слизистой оболочки мочеиспускательного канала, особенно на передней и боковых стенках его, располагаются гроздьевидные, трубчато-альвеолярные парауретральные железы, выделяющие слизистый секрет, количество которого увеличивается при половом возбуждении. Он служит для увлажнения уретры и вместе с секретом луковично-уретральных желез поддерживает щелочную реакцию, благоприятную для спермиев.
Семенной холмик - представляет собой возвышение на задней стенке предстательной части уретры, в середине которого располагается мужская маточка - рудимент мюллеровых протоков. Длина маточки - около 8-10 мм. В центре маточки, которая внедряется в толщу вещества предстательной железы, открывается щель, переходящая в неглубокую (до 4-6 мм) полость. На дне этой полости или ниже ее на семенном холмике открываются щелевидные устья семявыбрасывающих протоков. Семенной холмик состоит из пещеристой ткани, богатой эластическими волокнами и продольными пучками гладких мышц. По бокам семенного бугорка открываются (по 10-12 с каждой стороны)" устья выводных протоков долек предстательной железы.
Физиологическое значение семенного бугорка до конца не изучено. Будучи эмбриологически и анатомически связанным с органами половой системы, семенной бугорок активно участвует в акте эякуляции. Вокруг него концентрируются выводные протоки большинства половых желез и нервные окончания, связанные с центром эякуляции.
Мочеиспускательный канал у мужчин изменяется с возрастом. До периода полового созревания канал короче, уже и имеет резкий изгиб в заднем отделе. После полового созревания в связи с увеличением полового члена, развитием предстательной железы уретра формируется окончательно. В пожилом возрасте при гипертрофии парауретральных желез изменяется предстательный отдел мочеиспускательного канала и уменьшается его просвет.
Мочеиспускательный канал выполняет 3 функции: удерживает мочу в мочевом пузыре; проводит мочу при мочеиспускании; проводит семенную жидкость в момент эякуляции. Удержание в мочевом пузыре мочи осуществляется за счет внутреннего (непроизвольного) и наружного (произвольного) сфинктеров. При переполнении мочевого пузыря основную роль играет мощный наружный произвольный сфинктер, удерживать мочу помогает и сокращение мышечной массы предстательной железы. Мочеиспускание является сложным рефлекторно-произвольным актом. Когда внутрипузырное давление достигает определенного уровня (при объеме мочи в мочевом пузыре свыше 200 мл), появляется позыв к мочеиспусканию. Под влиянием волевого импульса происходит сокращение мышц мочевого пузыря и брюшной стенки с одновременным расслаблением сфинктеров, и мочевой пузырь опорожняется.
Проведение семенной жидкости по мочеиспускательному каналу осуществляется в момент эякуляции. Эякуляция - рефлекторный акт, в котором активное участие принимают сам мочеиспускательный канал и все образования, связанные с ним. При этом происходит сокращение внутреннего сфинктера, который вместе с набухшим во время эрекции семенным холмиком препятствует забрасыванию эякулята в мочевой пузырь. Одновременно с этим расслабляется наружный сфинктер и происходит последовательное опорожнение от содержимого придатков яичек, семявыносящих протоков, включая ампулярную часть, после чего возникает сокращение гладкой мускулатуры семенных пузырьков и предстательной железы, присоединяются мощные сокращения поперечнополосатой мускулатуры, седалищно-пещеристых и пещеристо-луковичных мышц и мышц тазового дна и промежности, в результате чего эякулят выбрасывается наружу со значительной силой. Регуляция акта эякуляции осуществляется симпатическим и парасимпатическим отделами нервной системы и под воздействием импульсов, следующих из Th XII -L IV и S II-IV сегментов спинного мозга.
Половой член является органом, который способен при возбуждении увеличиваться и приобретать значительную плотность, что необходимо для введения его во влагалище, совершения фрикций и подведения эякулята к шейке матки. В состоянии эрекции головка полового члена остается эластичной, что препятствует травмированию женских половых органов. Эрекция - рефлекторный акт, в основе которого лежит наполнение кровью кавернозных тел, имеющих многокамерное сетчатое строение. Г. Вагнер (1985) выделяет 4 фазы эрекции.
Фаза покоя характеризуется постоянным объемом полового члена, внутрипещеристым давлением и объемом крови в половом члене. В этом состоянии внутрипещеристое давление равно около 5 мм рт. ст., объем оттекающей крови - от 2,5 до 8 мл/мин и равен объему притекающей.
Фаза набухания проявляется увеличением объема полового члена, сопровождающимся постепенным возрастанием внутрипещеристого давления до 80-90 мм рт. ст. Продолжительность ее зависит от интенсивности сексуальной стимуляции, восприимчивости к ней и возраста мужины. При этом увеличивается приток артериальной крови до 90 мл/мин, а отток остается прежним.
Фаза эрекции определяется постоянным объемом напряженного полового члена, увеличением внутрипещеристого давления по меньшей мере до 80 мм рт. ст., достигающего уровня артериального.
Объем артериального притока крови в период наступления эрекции составляет от 120 до 270 мл/мин.
Фаза детумесценции проявляется исчезновением ригидности полового члена и уменьшением объема с постепенным возвращением к исходному уровню. Это достигается за счет резкого увеличения оттока крови до 40 мл/мин, одновременно с этим постепенно уменьшается приток и снижается внутрипещеристое давление.
В период набухания полового члена сохраняется отток крови по системе дорсальной вены, но увеличивается приток артериальной крови. В пожилом возрасте период набухания удлиняется, что, очевидно, объясняется ухудшением притока артериальной крови. Во время эрекции отток крови по системе дорсальной вены прекращается, вновь появляясь лишь при высоком внутрипещеристом давлении, и восстанавливается полностью после эякуляции в фазе детумесценции. Тем не менее во время эрекции ток крови сохраняется, что обеспечивает ее достаточную длительность при нереализованном половом акте. Эрекция регулируется при помощи парасимпатических волокон, идущих в составе n. erigentes, импульсами их крестцовых и спинномозговых центров, находящихся под контролем высших нервных центров коры головного мозга.
Половые железы (синоним гонады), органы, образующие половые клетки и половые гормоны. Являются составной частью половых органов. Выполняют смешанные функции, так как производят продукты не только внешней (потенциальное потомство), но и внутренней секреции, которые, попадая в кровяное русло, обеспечивают как нормальную жизнедеятельность организма человека в целом, так и его половую функцию. Закладка половых желёз, как и половых органов, происходит на протяжении первых 4 недель эмбриогенеза. Она обеспечивается одной Х-хромосомой, поэтому протекает одинаково у эмбриона (зародыша) с хромосомным набором 46,XX, 46,XY и 45,X. Ткань первичных половых желёз бисексуальна. Дифференцировка закладок в половые железы у эмбриона происходит с 4-й по 12-ю недели внутриутробного развития и на этом этапе полностью зависит от второй половой хромосомы - Y-хромосомы, контролирующей развитие зачатков гонад и половых органов по мужскому типу.
Морфология женских половых желез
Яичник (ovarium; греч. oophoron) - парный орган, женская половая железа, располагается в полости малого таза позади широкой связки матки. В яичниках развиваются и созревают женские половые клетки (яйцеклетки), а также образуются поступающие в кровь и лимфу женские половые гормоны. Яичник имеет овоидную форму, несколько уплощен в переднезаднем направлении. Цвет яичника розоватый. На поверхности яичника рожавшей женщины видны углубления и рубцы - следы овуляции и преобразования желтых тел. Масса яичника равна 5-8 г. Размеры яичника составляют: длина 2,5-5,5 см, ширина 1,5-3,0 см, толщина - до 2 см. У яичника различают две свободные поверхности: медиальную поверхность (facies medialis), обращенную в сторону полости малого таза, частично прикрытую маточной трубой, и латеральную поверхность (facies lateralis), прилежащую к боковой стенке малого таза, к слабовыраженному углублению - яичниковой ямке. Эта ямка находится в углу между покрытыми брюшиной наружными подвздошными сосудами вверху и маточной и запирательной артериями внизу. Позади яичника забрюшинно сверху вниз проходит мочеточник соответствующей стороны.
Поверхности яичника переходят в выпуклый свободный (задний) край (margo liber), спереди - в брыжеечный край (margo mesovaricus), прикрепляющийся посредством короткой складки брюшины (брыжейка яичника) к заднему листку широкой связки матки. На этом переднем крае органа находится желобоватое углубление - ворота яичника (hilum ovarii), через которые в яичник входят артерия и нервы, выходят вены и лимфатические сосуды. У яичника выделяют также два конца: закругленный верхний трубный конец (extremitas tubaria), обращенный к маточной трубе, и нижний маточный конец (extremitas utenna), соединенный с маткой собственной связкой яичника (lig. ovarii proprium). Эта связка в виде круглого тяжа толщиной около 6 мм идет от маточного конца яичника к латеральному углу матки, располагаясь между двумя листками широкой связки матки. К связочному аппарату яичника относится также связка, подвешивающая яичник (lig.suspensorium ovarii), являющаяся складкой брюшины, идущей сверху от стенки малого таза к яичнику, и содержащая внутри сосуды яичника и пучки фиброзных волокон. Яичник фиксирован короткой брыжейкой (mesovirium), которая представляет собой дупликатуру брюшины, идущую от заднего листка широкой связки матки к брыжеечному краю яичника. Сами яичники брюшиной не покрыты. К трубному концу яичника прикрепляется наиболее крупная яичниковая бахромка маточной трубы. Топография яичника зависит от положения матки, ее величины (при беременности). Яичники относятся к весьма подвижным органам полости малого таза.
Поверхность яичника покрыта однослойным зародышевым эпителием. Под ним залегает плотная соединительнотканная белочная оболочка (tunica albuginea). Соединительная ткань яичника образует его строму (stroma ovirii), богатую эластическими волокнами. Вещество яичника, его паренхиму, делят на наружный и внутренний слои. Внутренний слой, лежащий в центре яичника, ближе к его воротам, называют мозговым веществом (medulla ovarii). В этом слое в рыхлой соединительной ткани располагаются многочисленные кровеносные и лимфатические сосуды и нервы. Наружный слой яичника - корковое вещество (cortex ovarii) более плотный. В нем много соединительной ткани, в которой располагаются созревающие первичные фолликулы яичника (folhculi ovarici primarii), вторичные (пузырчатые) фолликулы (folhculi ovarici secundarii), a также зрелые фолликулы, граафовы пузырьки (folhculi ovarici maturis), а также желтые и атретические тела. В каждом фолликуле находится женская половая яйцеклетка, или овоцит (ovocytus). Яйцеклетка диаметром до 150 мкм, округлая, содержит ядро, большое количество цитоплазмы, в которой, помимо клеточных органелл, имеются белково-липидные включения (желток), гликоген, необходимые для питания яйцеклетки. Свой запас питательных веществ яйцеклетка обычно расходует в течение 12-24 ч после овуляции. Если оплодотворение не наступает, яйцеклетка погибает.
Яйцеклетка человека имеет две покрывающие ее оболочки. Кнутри находится цитолемма, которая является цитоплазматической мембраной яйцеклетки. Снаружи от цитолеммы располагается слой так называемых фолликулярных клеток, защищающих яйцеклетку и выполняющих гормонообразующую функцию - выделяют эстрогены. Возле каждого яичника расположены рудиментарное образование - придаток яичника, околояичник (придаток придатка), везикулярные привески, остатки канальцев первичной почки и ее протока.
У новорождённой девочки длина яичников составляет 0,5-3 см, они имеют цилиндрическую форму, гладкую поверхность и расположены высоко над входом в малый таз. К 5-7 годам яичники занимают обычное положение, приобретают яйцевидную форму. К 16 годам яичники значительно утолщаются, а длина увеличивается в среднем на 0,6 см.
В половом развитии девочек выделяют 3 периода: нейтральный (первые 5-6 лет), препубертатный (с 6 до 9-10 лет) и пубертатный (до наступления половой зрелости). В нейтральном периоде половые гормоны оказывают на рост и развитие ребёнка минимальное влияние. В пубертатном периоде под влиянием гонадотропных гормонов усиливается рост фолликулов, увеличивается синтез эстрогенов. В этом периоде меняется архитектоника тела, развиваются молочные железы, увеличиваются наружные и внутренние половые органы, изменяется структура эндометрия. При увеличенной концентрации эстрогенов наступает первая менструация (менархе), средние сроки появления которой составляют 12,5-13 лет.
Морфология мужских половых желез
Яичко (testis; греч. orchis, s.didymis) - парная мужская половая железа. Функцией яичек является образование мужских половых клеток и гормонов, поэтому яички одновременно еще и железы внешней и внутренней секреции.
Яички, или семенники, расположены в области промежности в особом вместилище - мошонке, причем левое яичко ниже правого. Они отделены друг от друга перегородкой мошонки и окружены оболочками. Поверхность каждого яичка гладкая, блестящая. Длина яичка в среднем составляет 4 см, ширина - 3 см, толщина - 2 см. Масса яичка равна 20- 30 г. Яичко имеет плотную консистенцию, овальную форму и несколько сплющено с боков. В нем различают две поверхности: более выпуклую латеральную поверхность и медиальную поверхность, а также два края: передний край (margo anterior) и задний край (margo posterior), к которому прилежит придаток яичка. У яичка выделяют верхний конец (extremitas superior) и нижний конец (extremitas inferior). На верхнем конце яичка часто встречается небольших размеров отросток - привесок яичка (appendix testis), являющийся рудиментом краниального конца парамезонефрального протока.
Снаружи яичко покрыто беловатого цвета фиброзной оболочкой, получившей название белочной оболочки (tunica albugmea). Под оболочкой находится вещество яичка - паренхима яичка (parenchyma testis). От внутренней поверхности заднего края белочной оболочки в паренхиму яичка внедряется валикообразный вырост соединительной ткани - средостение яичка (medidstinum testis), от которого веерообразно идут тонкие соединительнотканные перегородочки яичка (septula testis), разделяющие паренхиму на дольки яичка (lobuli testis). Последние имеют форму конуса и своими вершинами обращены к средостению яичка, а основаниями - к белочной оболочке. В яичке насчитывается от 250 до 300 долек. В паренхиме каждой дольки два-три извитых семенных канальца (tiibuli seminiferi contorti), содержащих сперматогенный эпителий. Каждый из канальцев имеет длину около 70-80 см и диаметр 150-300 мкм. Направляясь к средостению яичка, извитые семенные канальцы в области вершин долек сливаются друг с другом и образуют короткие прямые семенные канальцы (tiibuli seminiferi recti). Эти канальцы впадают в сеть яичка (rete testis), которая расположена в толще средостения яичка. Из сети яичка начинаются 12-15 выносящих канальцев яичка (ductuli efferentes testis), направляющихся в его придаток, где они впадают в проток придатка яичка. Извитые семенные канальцы выстланы сперматогенным эпителием и поддерживающими клетками (клетки Сертоли), расположенными на базальной мембране. Клетки сперматогенного эпителия, находящиеся на разных стадиях сперматогенеза, образуют несколько рядов. Среди них различают стволовые клетки, сперматогонии, сперматоциты, сперматиды и сперматозоиды. Сперматозоиды вырабатываются только в стенках извитых семенных канальцев яичка. Все остальные канальцы и протоки яичка являются путями выведения сперматозоидов.
Анатомо-физиологические особенности
У новорождённого масса яичка составляет 0,3 г, а размеры - 10x7 мм. К году размеры яичек увеличиваются до 14x9 мм, в 2-5 лет - 16x10 мм. К 10-11 годам длина яичка увеличивается в 2-2,5 раза (до 20-25 мм), а масса - до 2 г. У взрослого человека размеры яичка составляют 30-50x20-30 мм, а масса - около 20 г. У новорождённого семенные канальцы и канальцы сети не имеют просвета, который появляется к периоду полового созревания.
Половое развитие мальчиков делят на 3 периода: допубертатный (от 2 до 6-7 лет) - период гормонального покоя, препубертатный (от 6 до 10-11 лет), характеризующийся усилением синтеза андрогенов надпочечниками и формированием морфологических структур яичка, и пубертатный (с 11 - 12 лет), когда под влиянием тестостерона формируются вторичные половые признаки. Вначале появляются пигментация и множественные мелкие складки на мошонке, яички увеличиваются и опускаются на её дно, начинается рост полового члена, происходит оволосение лобка, появляются волосы в подмышечных областях, над верхней губой, на щеках, подбородке. Увеличивается гортань, происходит мутация голоса, изменяются размеры предстательной железы, постепенно усиливаются процессы сперматогенеза.
Большая часть циркулирующего тестостерона (60%) прочно связана в крови с глобулином, связывающим половые гормоны (ГСПГ). Свободный и связанный с альбумином тестостерон может поступать в клетки организма, в свете чего эту часть тестостерона называют биологически доступной. Несмотря на связывание с ГСПГ, у тестостерона непродолжительный период полураспада, составляющий 10 мин. Тестостерон метаболизируется главным образом печенью. Однако метаболиты тестостерона составляют только 20-30% 17-кетостероидов мочи.
ГСПГ - крупный гликопротеид, вырабатывается печенью. Продукция ГСПГ печенью зависит от многих метаболических факторов:
- половые стероиды активно модулируют синтез ГСПГ - эстрогены его стимулируют, в то время как андрогены подавляют, чем обусловлена более высокая концентрация ГСПГ у женщин;
- у больных циррозом печени уровень эстрогенов в крови остаётся нормальным, а тестостерона снижается, что ведёт к повышению уровня ГСПГ у таких больных;
- сниженная концентрация Т4 или Т, снижает уровень ГСПГ, в то время как на фоне тиреотоксикоза уровень ГСПГ повышается;
- концентрация ГСПГ снижена при ожирении и акромегалии, что обусловлено влиянием гиперинсулинемии.
Факторы, влияющие на концентрацию глобулина, связывающего половые гормоны
Превращение тестостерона в 17β-эстрадиол и дигидротестостерон (ДГТ) . Суточный синтез тестостерона составляет 5-7 мг, или 5000-7000 мкг. У здоровых мужчин образуется до 40 мкг 17β -эстрадиола, причём 3/4 этого количества образуется в периферических тканях путём ароматизации тестостерона ферментом ароматазой, а остальные 10 мкг секретируются непосредственно тестикулами (клетками Лейдига). Наибольшее количество ароматазы содержится в жировой ткани, поэтому чем выше степень ожирения, тем интенсивнее синтез эстрадиола.
Метаболизм эстрадиола у мужчин:
- суточная продукция 35-45 мкг;
- биологически активно 2-3% эстрадиола, остальной связан с ГСПГ;
- источники циркулирующего эстрадиола:
- образование из тестостерона путём его ароматизации на периферии - 60%;
- секреция тестикулами - 20%;
- периферическая конверсия из эстрона - 20%.
Основная часть ДГТ (до 350 мкг) образуется путём прямой трансформации тестостерона под действием 5α-редуктазы. У человека выделено два изофермента 5-редуктазы. Тип 1 локализуется преимущественно в коже, печени и тестикулах, в то время как тип II - в репродуктивных тканях, коже половых органов и придатке яичка.
Связывание с андрогеновыми рецепторами . Андрогеновый рецептор - полипептид (910 аминокислот), подобно другим стероидным и тиреоидным рецепторам относится к ДНК-связывающимся протеинам. Одни и те же рецепторы связывают тестостерон и ДГТ.
Регуляция функции мужских половых желёз
Функция тестикул регулируется замкнутыми системами обратной связи, в которых выделяют шесть основных компонентов:
- экстрагипоталамические отделы ЦНС;
- гипоталамус;
- аденогипофиз;
- тестикулы;
- регулируемые мужскими половыми гормонами органы-мишени;
- транспортная система для мужских половых гормонов и их метаболизм.
Экстрагипоталамическая регуляция ЦНС . Экстрагипоталамические отделы мозга оказывают на репродуктивную функцию как стимулирующее, так и подавляющее действие. В среднем мозге клетки содержат биогенные амины, норадреналин (НА) и серотонин (5-гидрокситриптамин; 5-ГТ), а также нейротрансмитеры, которые тесно связаны с многими отделами гипоталамуса, включая преоптическую, переднюю и медиобазальную зоны, где локализуются нейроны, вырабатывающие ГнРГ.
Гипоталамическая регуляция
- Пульсирующая секреция ГнРГ. Гипоталамус служит интегрирующим центром регуляции ГнРГ. ГнРГ - декапептид, который секретируется в портальную систему гипофиза с определённой периодичностью - пик секреции каждые 90-120 мин. Период полураспада ГнРГ составляет 5-10 мин, и в системный кровоток он практически не попадает, поэтому не исследуют его содержание в крови. От частоты пульсирующей секреции ГнРГ зависит избирательность стимулирования секреции гонадотропинов ЛГ и ФСГ. Регулирует секрецию ГнРГ «гипоталамический генератор биоритма», локализующийся в аркуатном ядре. Вместе с тем каждый отдельный нейрон секретирует ГнРГ не постоянно, а периодически, что и обеспечивает, вероятно, суммарный пульсирующий характер секреции ГнРГ под синхронизирующим влиянием «гипоталамического генератора биоритма». Пульсирующая секреция ГнРГ определяет и пульсирующий ритм секреции гормонов регулируемых им желёз (ЛГ, ФСГ, андрогенов, ингибина). Ранее предполагали, что существуют рилизинг гормоны как для ЛГ, так и для ФСГ, но в настоящее время большинством разделяется точка зрения, что регулирует секрецию как ЛГ, так и ФСГ только ГнРГ, причём степень влияния на ЛГ и ФСГ зависит от ритма секреции ГнРГ: высокая частота снижает секрецию как ЛГ, так и ФСГ; низкая частота в большей степени стимулирует секрецию ФСГ, чем ЛГ; введение ГнРГ с постоянной скоростью подавляет секрецию обоих гипофизарных гонадотропинов.
- Регуляция ГнРГ. Синтез и секрецию ГнРГ регулируют экстрагипоталамические отделы ЦНС, концентрация в крови андрогенов, пептидных гормонов, таких, как пролактин, активин, ингибин и лептин. Локальная модуляция секреции ГнРГ осуществляется нейропептидами, катехоламинами, индоламинами, NO, дофамином, нейропептидом Y, ВИН и КРГ.
Гипоталамический пептид кисспептин у мужчин стимулирует быстрое повышение секреции ЛГ. Совсем недавно было показано, что гипоталамическая секреция ГнРГ опосредуется кисснейронами, вырабатывающими кисспептин, который стимулирует кисс1-рецептор. Кисспептиновые нейроны также опосредуют обратную связь половых гормонов с гипоталамусом.
Введение лепитина повышает содержание кисс1 в матричной РНК клеток гипоталамуса, так же как и секрецию ЛГ и тестостерона. Кисспептин поэтому может быть промежуточным звеном в реализации стимуляции лептином секреции ГнРГ.
Пролактин подавляет секрецию ГнРГ, что проявляется гипогонадизмом у пациентов с гиперпролактинемией.
Гипофизарная регуляция. Гонадотропины ЛГ и ФСГ синтезируются гонадотрофами аденогипофиза и секретируются пикообразно, в ответ на пикообразную секрецию ГнРГ. Однако, поскольку скорость элиминации гонадотропинов более низкая, чем ГнРГ, то пики секреции гонадотропинов менее выражены. ЛГ и ФСГ - крупные гликопротеиды.
ЛГ связывается специфическими мембранными рецепторами клеток Лейдига, что запускает цепь реакций, опосредуемых G-протеином и приводящих к стимуляции синтеза тестостерона в тестикулах.
ФСГ связывается с рецепторами на клетках Сертоли, стимулируя в них образование ряда специфических белков, включая андроген-связывающий протеин, ингибин, активин, активатор плазминогена, γ-глутамилтранспептидазу и ингибитор протеинкиназы. ФСГ в содружестве с тестостероном, продуцируемым клетками Лейдига, и активином синергично стимулируют сперматогенез и подавляют апоптоз половых клеток.
Регуляция секреции гонадотропинов . Как было указано выше, секреция гонадотропинов регулируется пульсирующей секрецией ГнРГ.
Регулирующее влияние цитокинов воспаления .
Биологическое действие тестостерона и его метаболитов
Тестостерон оказывает прямое влияние на организм или опосредованное, через два основных своих метаболита - ДГТ и 17β-эстрадиол.
Выделяют три этапа жизни, на которых тестостерон оказывает различное, причём ключевое, влияние на организм. Недостаток тестостерона или 5а-редуктазы, превращающей тестостерон в ДГТ, приводит к развитию амбивалентных половых органов.
При отсутствии фермента 5α-редуктазы появляется такой симптом, как микропенис. ДГТ необходим для роста и развития предстательной железы, где его концентрация в 10 раз выше, чем тестостерона. В принципе действия тестостерона и ДГТ топографически зависимы: на рост бороды влияет тестостерон, а оволосение подмышек и лобка - ДГТ-зависимое. ДГТ подавляет рост волос на голове, что вызывает характерное облысение у некоторых мужчин. Тестостерон стимулирует эритропоэз через два механизма:
- стимулируя почечное и внепочечное образование эритропоэтина;
- оказывая прямое влияние на костный мозг.
При дефиците фермента ароматазы развивается остеопороз, так как понижается содержание эстрадиола. Эстрадиол также необходим для закрытия зон эпифизального роста.
В последнее время появились данные относительно влияния тестостерона на обмен веществ:
- повышает чувствительность к инсулину и, соответственно, толерантность к глюкозе, стимулирует митохондриальные гены окислительного фосфорилирования;
- повышает экспрессию регуляторных ферментов гликолиза и транспортёра глюкозы GLUT4;
- эффект тестостерона на липиды проявляется после завершения пубертатного периода: снижается концентрация липопротеинов высокой плотности, а триглицеридов и липопретеинов низкой плотности - повышается;
- в препубертатном периоде половых различий в липидном обмене нет.
Тестостерон обладает сосудорасширяющим действием, причём эндотелиально-независимым, оказывая прямое действие на гладкую мускулатуру сосудов. Эстрадиол также обладает сосудорасширяющим действием, которое реализуется через оксид азота (II).
Тестостерон обладает важным психотропным действием на мозг, повышая настроение (драйв), мотивацию, агрессивность и либидо. Он влияет и на когнитивные функции, в частности улучшает пространственное ориентирование и математические способности. Однако уровень тестостерона негативно коррелирует с лёгкостью вербальной функции.
Биологические эффекты тестостерона и дигидротестостерона
| Тестостерон | ДГТ |
|---|---|
| Стимулирует рост бороды. Недостаток приводит к эректильной дисфункции | Обеспечивает внутриутробное развитие мужских половых органов |
| Повышает либидо. Обеспечивает нормальную архитектонику полового члена | Вызывает облысение |
| Стимулирует развитие мышечной ткани и её силы | Стимулирует рост и развитие предстательной железы |
| Стимулирует эритропоэз | |
| Повышает чувствительность к инсулину | |
| Повышает толерантность к глюкозе | |
| Повышает экспрессию регуляторных ферментов гликолиза | |
| Повышает экспрессию транспортёра глюкозы GLUT4 | |
| Обладает сосудорасширяющим действием | |
| Повышает настроение (драйв) | |
| Улучшает функцию мозга, в частности кратковременную память, и повышает математические способности | |
| Уровень тестостерона отрицательно коррелирует с вербальными функциями |
В пубертатном периоде тестостерон и ДГТ оказывают влияние на рост мошонки, полового члена и обеспечивают функциональное единство этих структур, а также они стимулируют:
- амбисексуальный рост волос;
- сексуальный рост волос (бороды, усов, на грудной клетке, животе и спине);
- активность сальных желёз (акне).
Тестостерон и ДГТ стимулируют рост скелетной мускулатуры и гортани, что в последнем случае проявляется низким голосом у мужчин.
Тестостерон и его метаболиты (ДГТ и эстрадиол) стимулируют рост эпифизарных хрящевых пластинок, вызывают быстрый рост в пубертатном возрасте, способствуют закрытию зон роста эпифиза, повышают костную массу, стимулируют гемопоэз, рост предстательной железы, либидо, меняют характерным образом социальное поведение, повышают агрессивность.
Эстрадиол:
- обеспечивает пубертатный рост;
- поддерживает плотность костной массы;
- регулирует секрецию гонадотропинов.
Фазы функционального становления гипоталамогипофизарногонадной системы
У плода мужского пола концентрации гонадотропинов и тестостерона в крови начинают возрастать к концу 2-го месяца гестации, быстро повышаясь до максимума, который поддерживается вплоть до поздних сроков беременности; концентрация тестостерона у новорождённых мальчиков лишь незначительно превышает наблюдаемую у девочек.
Вскоре после родов у мальчиков концентрации ЛГ, ФСГ и тестостерона снова повышаются и держатся на достигнутом уровне около 3 мес, но затем постепенно снижаются до очень низкого уровня к концу первого года жизни. Такие низкие уровни гонадотропинов и тестостерона сохраняются вплоть до пубертатного периода.
В препубертатный период секреция ГнРГ увеличивается по амплитуде и частоте в утренние часы перед пробуждением, что сопровождается повышением в утренние часы секреции ЛГ, ФСГ и тестостерона. С развитием пубертатного периода продолжительность пикообразной секреции гонадотропинов и тестостерона увеличивается, пока в конце пубертата пики секреции не становятся регулярными в течение суток.
В пубертатный период восстанавливается и чувствительность гонадотропинов к стимулирующему действию ГнРГ.
После наступления пубертата концентрации гонадотропинов и тестостерона повышаются, достигая значений взрослого мужчины к 17 годам.
Стадии пубертатного периода у мальчиков (по Таннеру)
| Стадии развития половых органов | Стадии оволосения лобка |
| Стадия 1 . Препубертатная. Тестикулы, мошонка и половой член приблизительно одинакового размера и пропорции,характерные для раннего детства | Стадия 1 . Препубертатная. Заметен рост только пушковых волос, который выражен не в большей степени, чем на передней стенке живота, т.е. оволосение лобка отсутствует |
| Стадия 2 . Мошонка и тестикулы увеличиваются, меняется текстура кожи мошонки, она приобретает красноватый оттенок | Стадия 2 . Рост вокруг основания полового члена длинных, слегка пигментированных, редких, пушковых, прямых или слегка вьющихся волос |
| Стадия 3 . Происходит рост полового члена, сначала главным образом в длину и в меньшей степени - в диаметре. Также отмечается дальнейший рост мошонки и тестикул | Стадия 3 . Волосы становятся значительно темнее, грубее, более извитыми. Происходит рост редких волос надлобковым сочленением |
| Стадия 4 . Половой член ещё больше увеличивается по длине и в диаметре, развивается головка полового члена. Увеличиваются тестикулы и мошонка, темнеет кожа мошонки | Стадия 4 . Полное оволосение лобка, как у взрослого, но покрываемая поверхность заметно меньше, чем у большинства взрослых. |
| Стадия 5 . Полное развитие половых органов как по размеру, так и по форме. После достижения 5-й стадии развития дальнейшего роста половых органов не происходит | Стадия 5 . Волосы на лобке как по качеству, так и по типу соответствуют взрослому периоду, распределены в виде повёрнутого вершиной вниз треугольника. Оволосение также отмечается и на внутренней поверхности голеней, но не вдоль белой линии живота и не распространяется над основанием треугольника роста волос на лобке. У большинства мужчин с возрастом происходит дальнейшее распространение роста волос над лобком |
В допубертатный период уровень гонадотропинов и стероидов гонад низкий. Вместе с тем под влиянием АКТГ секреция андрогенов надпочечников начинает повышаться у мальчиков с 7-8 лет, т.е. Это явление называют адренархе. Наблюдаемый до пубертата скачок роста и иногда появление подмышечных и лобковых волос связаны с действием андрогенов надпочечников.
Рост волос на лобке вызывают андрогены тестикул и надпочечников. Усиливается рост волос и на лице: рост распространяется к середине нижней губы, на боковые и нижнюю поверхность подбородка. Первая стадия роста волос на лице совпадает с 3-й стадией оволосения лобка (в среднем возраст 14,5 лет), а последняя стадия - с завершением 5-й стадии оволосения лобка и 5-й стадии развития половых органов. Волосы в перианальной зоне появляются немного раньше, чем в подмышечных впадинах. В конце и после пубертата зона роста волос распространяется из лобковой области вверх, принимая ромбовидные очертания.
Первым признаком наступления пубертатного периода обычно бывает увеличение максимального диаметра тестикул (исключая эпидидимис) более 2,5 см. В созревающих клетках Сертоли прекращаются митозы, и они дифференцируются в зрелые клетки. Под влиянием ЛГ число клеток Лейдига в тестикулах также увеличивается.
Сперматозоиды в утренней моче (спермархе) появляются в хронологическом возрасте 13,5 года или при соответствующем костном возрасте на 3-4 стадии развития половых органов и оволосения лобка на 2-4 стадии. Когда пубертат развивается раньше или позже, то соответственно меняется и возраст наступления спермархе. Таким образом, репродуктивная функция у мальчиков развивается раньше наступления физической и, естественно, психологической зрелости.
Пубертатное ускорение (скачок) роста происходит под многосторонним эндокринным контролем, в котором ведущая роль отводится СТГ и половым гормонам; при недостатке одного из них или обоих пубертатный скачок роста уменьшается или не происходит вовсе. Усиливая секрецию СТГ, половые гормоны опосредованно стимулируют синтез ИРФ-1 и, кроме того, непосредственно активизируют образование ИРФ-1 в хрящах. С начала пубертата скорость роста ног опережает скорость роста туловища, но в период скачка роста эти скорости выравниваются. Дистальные части конечностей (стопы и кисти) начинают расти до начала роста проксимальных частей, поэтому быстрое увеличение размера обуви - первый предвестник пубертатного скачка роста. В среднем за пубертатный период мальчики вырастают на 28 см, и чем позже начинается пубертатный период, тем окончательный рост оказывается выше (за счёт более продолжительного периода пубертата).
В пубертате увеличивается гортань, утолщаются и удлиняются голосовые связки, что сопровождается приблизительно в 13-летнем возрасте ломкой голоса и снижением его тембра, завершается формирование мужского тембра к 15 годам. За счёт анаболического действия андрогенов нарастает масса мышц (особенно андроген-чувствительных мышц грудной клетки и плечевого пояса), соединительной ткани, костей, возрастает плотность костной ткани. Максимальной массы лимфоидная ткань достигает к 12 годам, а после этого масса снижается с прогрессированием пубертата.
